 |
L’iontophorèse utilise le passage d’un faible courant (< 0,5 mA/cm2) à travers la peau. Cette technique permet de délivrer des molécules à travers la peau dans un but thérapeutique ou d’en extraire pour un but diagnostique (iontophorèse inverse). |
Elle est couramment utilisée depuis plusieurs dizaines d’années dans différentes applications: par les kinésithérapeutes pour des tendinites, etc. (avec des AINS ou des corticoïdes), lors de test de sueur (avec de la pilocarpine pour stimuler les glandes sudoripares), dans le traitement des sudations excessives, et en ophtalmologie pour le traitement des infections bactériennes ou virales cornéennes profondes ou pour transférer des produits qui ne franchissent pas la barrière cornéenne.
Dans le domaine de la douleur, les premières publications de lidocaïne (Xylocaïne®) par iontophorèse (en général associée à de l’adrénaline), datent d’une quarantaine d’années ; la Food and Drug Administration a approuvé cette technique en décembre 1995.
Un dispositif pour l’administration du fentanyl est à l’étude, d’autres antalgiques telle la nalbuphine ont également fait l’objet de publications.
Chez l’enfant, un des premiers essais contrôlés randomisés a été publié en 1991 (cf. infra).
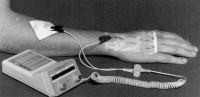
En pratique, un mélange de lidocaïne à 1 % ou le plus souvent 2 %, et d’adrénaline à 1:100 000 imprègne un support placé sur une électrode. Cette électrode est appliquée sur la zone à anesthésier, une électrode de polarité différente étant placée à distance. Un générateur de courant relie ces 2 électrodes et permet de régler l’intensité et la durée du courant administré.
La durée d’application est le plus souvent de 10 minutes, l’intensité du courant variable selon les études.
Les principaux effets indésirables, fonction de l’intensité du courant délivré, sont des sensations de fourmillement, de prurit, de chaleur, un érythème et rarement une brûlure.
Divers dispositifs existent, le seul disponible en France, actuellement, étant le Phoresor® dont l’utilisation est limitée par le coût des électrodes à usage unique (environ 15 euros).
Il est néanmoins possible d’utiliser cette technique avec d’autres appareils de physiothérapie plus complets, et onéreux, qui ne sont pas dédiés à la seule iontophorèse.
Evaluation d’une dose faible de lidocaïne par iontophorèse pour une anesthésie topique chez l’enfant et l’adulte: un essai contrôlé randomisé
Evaluation of a low-dose lidocaine iontophoresis system for topical anesthesia in adults and children: a randomized, controlled trial.
Zempsky WT, Sullivan J, Paulson DM, Hoath SB
Clin Ther 2004 Jul; 26(7): 1110-19
| Cette étude prospective, multicentrique, randomisée en double aveugle contre placebo, évalue l’efficacité de la lidocaïne par iontophorèse à doses faibles, lors d’une ponction veineuse chez l’enfant ou chez l’adulte (lors d’un prélèvement ou de la pose d’un cathéter veineux). 276 adultes et 272 enfants âgés de 5 à 17 ans participent à cette étude. La lidocaïne par iontophorèse est appliquée pendant 10 minutes avant la ponction à des doses inférieures à celles habituellement utilisées. Dans le groupe placebo la lidocaïne est remplacée par du sérum physiologique. La douleur est évaluée par l’EVA chez les enfants de plus de 12 ans et les adultes, et par une échelle de visage (Facial Affective Scale) chez tous les enfants. Quel que soit l’âge, les scores de douleur sont moindres dans le groupe lidocaïne. |
Administration percutanée de lidocaïne par un nouveau système de iontophorèse chez l’enfant: tolérance et absence de biodisponibilité systémique
Percutaneous lidocaine administration via a new iontophoresis system in children: tolerability and absence of systemic bioavailability
Kearns GL, Heacook J, Daly SAJ, Singh H, Alander SW, Qu S.
Pediatrics 2003; 112; 578-82
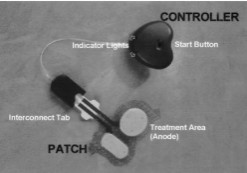 |
Cette étude a pour but d’évaluer la tolérance et la biodisponibilité systémique de la lidocaïne délivrée par iontophorèse à l’aide d’un nouveau dispositif: Nortstar Iontophoretic Patch (Becton Dickinson Transdermal System). Ce système, différent des autres, comprend un réservoir (l’anode) recueillant la lidocaïne à 10 % et l’adrénaline à 0,1 %, délivrées pendant 10 minutes avec un courant de 1,78 mA. Les 12 enfants recrutés sont âgés de 5 à 15 ans. 3 tests sont effectués à H0, H3 et H3 1/2. Un cathlon a été initialement posé afin de permettre des prélèvements sanguins à des temps déterminés. Les 3 tests sont effectués sur 3 sites parmi les 4 proposés : pli du coude, thorax antérieur, dorsal haut, et dos de la main. L’érythème et l’œdème sont évalués à H10 et H24 avec le score de Draize. Résultats: la technique a toujours été bien tolérée par les enfants, les réactions locales sont rares et mineures et semblent moins fréquentes pour les applications au niveau du pli du coude et de la main. Il n’a jamais été retrouvé des taux sanguins de lidocaïne supérieurs à 10 ng/mL, quel que soit le temps du prélèvement. Les taux étaient inférieurs au seuil de détection (0,5 ng/mL) pour 11 enfants et à 8,9 ng/mL pour le douzième, 5 min après le 3e test (les taux nécessaires à l’obtention d’un effet thérapeutique étant compris entre 1 500 et 5 500 ng/mL !). |
Lidocaïne par iontophorèse pour la ponction veineuse en pédiatrie : une étude
A study of lidocaine iontophoresis for pediatric venipuncture
Rose JB, Galinkin JL, Jantzen EC, Chiavacci RM.
Anesth Analg 2002; 94: 867-71, 16, eng
Dept. Anesthesiol., Child. Hosp., 34th St. Civic Ctr. Blvd., Philadelphia, PA 19104, USA
| Etude contrôlée randomisée, en double aveugle, portant sur 59 enfants âgés de 6 à 17 ans devant subir une ponction veineuse. 40 enfants reçoivent de la lidocaïne à 2 % (plus adrénaline à 1:100 000) administrée par iontophorèse ; 19 autres (groupe placebo) reçoivent la même préparation sans lidocaïne. La douleur est évaluée à l’aide d’une EVA par le patient, un parent et l’infirmière. Le score médian (en mm) de l’EVA du patient dans le groupe traité est de 7 (2-20,8) et de 31 (12-48) pour le groupe placebo. Les scores de satisfaction sont meilleurs dans le groupe traité. Le temps nécessaire à la délivrance du produit est inférieur à 10 minutes (8,8 ± 2,1 min).10/59 enfants rapportent des effets secondaires modérés (démangeaisons, pétéchies et ecchymoses, sensation de brûlure). Les effets secondaires observés semblent moins fréquents que lors d’études précédentes probablement du fait d’intensités électriques iontophorétiques moindres (20 mA/min versus 30-40 mA/min). L’anesthésie locale de lidocaïne par iontophorèse semble donc efficace, rapide et bien tolérée pour prévenir la douleur engendrée par les ponctions veineuses chez l’enfant. |
Lidocaïne par iontophorèse versus EMLA® pour la pose d’un cathéter veineux périphérique
Lidocaine iontophoresis versus eutectic mixture of local anesthetics (EMLA®) for IV placement in children
Galinkin JL, Rose JB, Harris K, Watcha MF.
Anesth Analg 2002; 94: 1484-8, 23, eng
Dept. Anesth. Crit. Care, Child. Hosp., 34th St. Civic Ctr. Blvd, Philadelphia, PA 19104-4399, USA
| Etude croisée prospective randomisée comparant la lidocaïne par iontophorèse à la crème EMLA® lors de la pose de cathéter veineux périphérique. 22 enfants, âgés de 7 à 16 ans, devant être perfusés à au moins 3 reprises, participent à l’étude. Ils sont randomisés pour recevoir alternativement EMLA® ou lidocaïne par iontophorèse. Le délai minimum est de 7 jours entre les 2 procédures. Lors d’une 3e perfusion, l’enfant choisit la méthode qu’il a préférée. 2,5 g d’EMLA® sont appliqués sur 2 sites pendant au moins 60 min et sont recouverts de Tegaderm®. Le courant initial de la iontophorèse est de 0 mA puis augmenté de 4 mA toutes les 60 secondes. le traitement est arrêté quand une dose de 40 mA/min a été délivrée. La douleur est évaluée par l’enfant et ses parents à l’aide d’une EVA. Un observateur, ignorant le traitement utilisé, évalue la douleur à l’aide de l’échelle Cheops ; il mesure également la FC avant, pendant et juste après le geste. Un score de satisfaction en 5 points est proposé à l’enfant, aux parents, à l’observateur et à la personne qui a posé le cathéter. 2 enfants n’ont pas supporté (démangeaisons, prurit) la iontophorèse et la dose de 40 mA/min n’a pu être atteinte. Il n’y a pas de différence entre les 2 groupes tant pour les scores de douleur (EVA et Cheops) que pour la difficulté du geste et les variations de la FC. Lors de la 3e perfusion, 50 % choisissent la iontophorèse, 23 % préfèrent EMLA® et 27 % n’ont pas de préférence. galinkin@email.chop.edu |
Essai clinique randomisé de l’anesthésie cutanée par iontophorèse pour la pose de cathéter intraveineux court chez l’enfant
A randomized clinical trial of dermal anesthesia by iontophoresis for peripheral intravenous catheter placement in children
Kim MK, Kini NM, Troshynski TJ, Hennes HM.
Ann Emerg Med 1999; 33 (4): 395-9, 11, eng
Section Emerg. Med., Dept. Pediatr., Med. Coll. Wisconsin, 8701 Watertown Plank Rd., Milwaukee, WI 53226-0509, USA
| Etude prospective randomisée en double aveugle chez des enfants de plus de 7 ans nécessitant une perfusion aux urgences. Administration par iontophorèse soit de lidocaïne avec épinéphrine (22 enfants) soit de placebo avec épinéphrine (25 enfants). Durée : 3 minutes courant 3 mA. Evaluation par EVA plus évaluation de l’inconfort lié à l’iontophorèse. EVA 0,5/10 dans le groupe lidocaïne contre 4 dans le groupe placebo. 57 % des enfants disent que la technique est légèrement inconfortable, 39 % n’ont rien senti, 4 % disent que c’est inconfortable. |
Anesthésie topique avec iontophorèse de Xylocaïne® pour la pose de perfusion chez l’enfant
Lidocaine iontophoresis for topical anesthesia before intravenous line placement in children
Zempsky WT, Anand KJ, Sullivan KM, Fraser D, Cucina K.
J Pediatr 1998; 132: 1061-3, 12, eng
Div. Pediatr. Emerg. Med., Connecticut Child. Med. Ctr., 282 Washington St., Hartford, CT 06106, USA
| Etude randomisée contre placebo portant sur 42 enfants (7-18 ans). L’iontophorèse (transfert de molécules au sein de tissus biologiques grâce à un courant électrique) favorise la pénétration cutanée de l’anesthésique local (Xylocaïne® à 2 %). Durée d’application : 30 min. Les scores EVA des patients passent de 58,5/100 (médiane) à 14,5/100. |
Anesthésie dermique : comparaison entre EMLA® et anesthésie locale par iontophorèse
Dermal anaesthesia : comparison of EMLA® cream with iontophoretic local anesthesia
Irsfeld S, Klement W, Lipfert P.
Br J Anaesth 1993; 71: 375-8, 21, eng
Dept. Clin. Anaesth., Heinrich-Heine-Univ., Moorenstr. 5, 4000 Dusseldorf, DEU
| Etude sur 6 volontaires sains : comparaison de l’action de la crème EMLA® et de Xylocaïne® 5% appliquée par iontophorèse (action d’un mini courant électrique qui augmente la pénétration transdermique). Pas de différence pour la douleur de pénétration cutanée, la douleur de l’injection d’un sérum hypertonique est abolie chez 5 sujets sur 6 avec la Xylocaïne® et chez aucun avec EMLA®. |
Iontophorèse de lidocaïne pour l’anesthésie de la chirurgie au laser dans le traitement de taches lie de vin
Iontophoresis of lidocaine for anesthesia during pulsed dye laser treatment of port-wine stains
Kennard CD, Whitaker DC.
J Dermatol Surg Oncol 1992; 18 (4): 287-94, 23, eng
Dept.Dermatol., Univ.Iowa Hosp.Clin., Iowa City, IA 52240, USA
Iontophorèse et injection sous-cutanée : comparaison de ces deux méthodes d’anesthésie locale chez l’enfant
Iontophoresis versus subcutaneous injection: a comparison of two methods of local anesthesia delivery in children
Zeltzer L, Regalado M, Nichter LS, Barton D, Jennings S, Pitt L.
Pain 1991; 44 (1): 73-8, 20, eng
Div.Child Dev.Biobehav.Pediatr., Dept.Pediatr.UCLA Sch.Med., 10833 Le Conte Ave., Los Angeles, CA 90024-1752, USA
L’étude concerne 14 enfants de plus de 9 ans en dialyse rénale chronique pour la mise en place de l’aiguille de dialyse au travers de la fistule. Chaque enfant est son propre témoin et l’évaluation est faite par EVA. L’analgésie est soit délivrée par injection sous-cutanée de lidocaïne, soit par iontophorèse, c’est-à-dire pénétration d’un gel de lidocaïne par application, pendant 10 minutes, d’un courant de 3 mA. Ni l’anxiété, ni le vécu douloureux ne sont différents (jugés par l’enfant). La réduction de la douleur est jugée plus importante par le personnel avec la iontophorèse. Aucune complication dans les 2 cas.
|
